La segunda ley de la termodinámica tiene varias formas de expresión. Una de ellas afirma que ninguna máquina térmica es capaz de convertir completamente toda la energía que absorbe en trabajo utilizable. Otra manera de enunciarla es decir que los procesos reales ocurren en un sentido tal, que la calidad de la energía es menor porque la entropía tiende a aumentar.
No es posible que el calor fluya desde un cuerpo frío hacia un cuerpo mas caliente, sin necesidad de producir ningún trabajo que genere este flujo. La energía no fluye espontáneamente desde un objeto a baja temperatura, hacia otro objeto a mas alta temperatura.
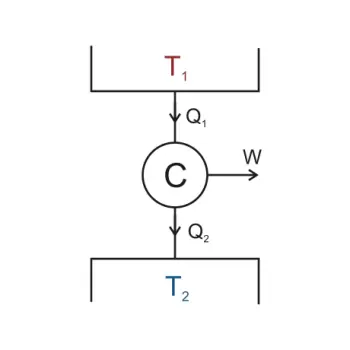
EJEMPLOS
1.la taza de café mañanero que espera tranquilamente sobre la mesa intercambiando calor con el entorno.
El café se enfría conforme pasa el tiempo, hasta quedar en equilibrio térmico con el ambiente, así que sería muy sorprendente que un día pasara lo contrario y el ambiente se enfriara mientras que el café se calentara por sí mismo.

2. Cuál es la eficiencia de una máquina térmica a la cual se le suministrarán 8 000 calorías para obtener 25 200 Joules de calor de salida?
SOLUCIÓN
Tenemos que convertir las calorías en Joules, y nos referimos a las calorías que se suministran:
Ahora si podemos sustituir nuestros datos en la fórmula:
Sustituyendo nuestros datos:
El valor de 0.25 lo multiplicamos por 100, para obtener el porcentaje de la eficiencia térmica:
Lo que sería equivalente a un 25% de eficiencia térmica.
No hay comentarios:
Publicar un comentario